Lý thuyết Hóa 9 Bài 28: Các oxit của cacbon
Bài giảng Hóa 9 Bài 28: Các oxit của cacbon
I. Cacbon oxit
– Công thức phân tử: CO.
– Phân tử khối: 28
1. Tính chất vật lí
CO là chất khí, không màu, không mùi, hơi nhẹ hơn không khí (dCOkk=2829), rất độc, ít tan trong nước.
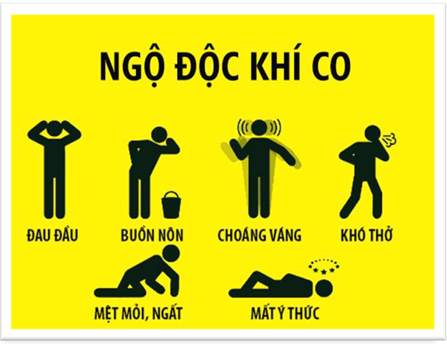
Hình 1: Biểu hiện của ngộ độc khí CO
2. Tính chất hóa học
a. CO là oxit trung tính
Ở điều kiện thường không phản ứng với nước, kiềm và axit.
b. CO là chất khử
– Ở nhiệt độ cao, cacbon oxit khử được các oxit của kim loại đứng sau nhôm trong dãy hoạt động hóa học để thu được kim loại.
Ví dụ:
CO + CuO (màu đen) →t0 CO2 + Cu (màu đỏ)
3CO + Fe2O3 →t0 2Fe + 3CO2
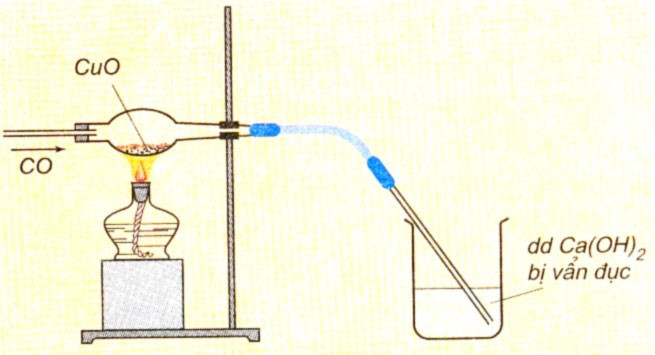
Hình 2: CO khử CuO
– CO cháy trong oxi hoặc trong không khí với ngọn lửa màu xanh, tỏa nhiều nhiệt.
Phương trình hóa học: 2CO + O2 →t0 2CO2
3. Ứng dụng
Khí CO được dùng làm nhiên liệu, chất khử… trong công nghiệp. Ngoài ra còn được dùng làm nguyên liệu trong công nghiệp hóa học.
II. Cacbon đioxit
– Công thức phân tử: CO2
– Phân tử khối: 44
1. Tính chất vật lí
– CO2 là chất khí, không màu, không mùi, nặng hơn không khí (dCO2KK=4429), không duy trì sự sống và sự cháy.
– CO2 bị nén và làm lạnh thì hóa rắn được gọi là nước đá khô (tuyết cacbonic). Nước đá khô được dùng để bảo quản thực phẩm.
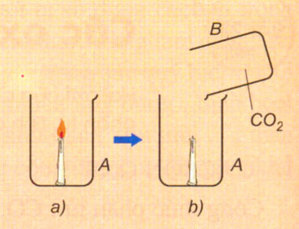
Hình 3: CO2 không duy trì sự cháy
2. Tính chất hóa học
CO2 là một oxit axit.
a. Tác dụng với nước tạo thành axit cacbonic
Phương trình hóa học:
CO2 + H2O →t0 H2CO3
Hình 4: Khí CO2 phản ứng với nước
Chú ý: CO2 phản ứng với nước tạo thành dung dịch axit, làm quỳ tím chuyển sang màu đỏ. H2CO3 không bền, dễ phân hủy thành CO2 và nước, khi đun nóng dung dịch thu được sẽ lại làm quỳ màu đỏ chuyển sang màu tím.
b. Tác dụng với dung dịch bazơ
Khí CO2 tác dụng với dung dịch bazơ tạo thành muối và nước. Tùy theo tỉ lệ số mol giữa CO2 và dung dịch bazơ mà có thể tạo ra muối trung hòa, muối axit hay hỗn hợp hai muối.
Ví dụ:
CO2 + 2NaOH → Na2CO3 + H2O
1 mol 2 mol
CO2 + NaOH → NaHCO3
1 mol 1 mol
c. Tác dụng với oxit bazơ
CO2 tác dụng với oxit bazơ (tan) tạo thành muối.
Ví dụ:
CO2 + CaO →t0 CaCO3
3. Ứng dụng
CO2 được dùng để chữa cháy, bảo quản thực phẩm.
Ngoài ra, CO2 còn được dùng trong sản xuất nước giải khát có gas, sản xuất sođa, phân đạm,…
Trắc nghiệm Hóa học 9 Bài 28: Các oxit của cacbon
Câu 1: CO có tính chất
A. Oxit axit, chất khí độc, có tính khử mạnh
B. Chất khí không màu, rất độc, oxit bazơ
C. Chất khí không màu, rất độc, oxit trung tính, có tính khử mạnh
D. Chất khí, không màu, không mùi, có tính oxi hóa mạnh
Câu 2: Cho khí CO2 tan vào nước cất có pha vài giọt quỳ tím. Dung dịch có màu nào?
A. Không màu
B. Đỏ
C. Xanh
D. Tím
Câu 3: Khử hoàn toàn 2,4 gam đồng(II) oxit bằng khí CO. Thể tích khí CO cần dùng (đktc) là
A. 0,224 lít
B. 0,672 lít
C. 0,448 lít
D. 0,560 lít
Câu 4: Tính chất hóa học của CO2 là
A. Tác dụng với nước
B. Tác dụng với dung dịch bazơ
C. Tác dụng với oxit bazơ
D. Cả A, B, C đều đúng
Câu 5: Khí CO không khử được oxit nào sau đây ở nhiệt độ cao?
A. CuO
B. ZnO
C. PbO
D. CaO
Câu 6: Khử hoàn toàn 6,4 gam Fe2O3 bằng khí CO dư. Sản phẩm khí thu được cho vào bình đựng nước vôi trong dư thu được m gam kết tủa màu trắng. Giá trị của m là
A. 10 gam
B. 11 gam
C. 12 gam
D. 14 gam
Câu 7: Ứng dụng của CO2 được dùng để
A. Chữa cháy
B. Bảo quản thực phẩm
C. Dùng trong sản xuất nước giải khát có gas, sản xuất sođa, phân đạm, …
D. A, B, C đều đúng
Câu 8: Điều nào sau đây không đúng cho phản ứng của CO và O2
A. Phản ứng tỏa nhiệt
B. Phản ứng thu nhiệt
C. Phản ứng không xảy ra ở điều kiện thường
D. Phản ứng kèm theo sự giảm thể tích
Câu 9: Cho 1,12 lít khí CO ở đktc tác dụng vừa đủ với 4 gam oxit MO nung nóng. Kim loại M là
A. Fe
B. Mg
C. Zn
D. Cu
Câu 10: Khí CO có ứng dụng trong lĩnh vực nào sau đây?
A. Nhiên liệu trong công nghiệp
B. Chất khử trong công nghiệp luyện kim
C. Nguyên liệu trong công nghiệp hóa chất
D. Cả A, B, C đều đúng
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 9 đầy đủ, chi tiết khác:
Lý thuyết Bài 29: Axit cacbonic và muối cacbonat
Lý thuyết Bài 30: Silic. Công nghiệp silicat
Lý thuyết Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Lý thuyết Bài 32: Luyện tập chương 3: phi kim – Sơ lược về bảng tuần hoàn
Lý thuyết Bài 34: Khái niệm về hợp chất hữu cơ và hóa học hữu cơ
